Un nuevo estudio en Nature-Cancer evitó con éxito el crecimiento del neuroblastoma en ratones modificando las células CAR-T. Esto significa que las células CAR-T que generalmente solo tienen un buen efecto sobre los tumores hematológicos también pueden desempeñar un papel en los tumores sólidos.
Esto no solo significa que el neuroblastoma puede tratarse con CAR-T, y si se siguen las ideas del estudio, quizás finalmente se romperá el confinamiento de CAR-T en tumores sólidos.
Necesitamos saber que el receptor de antígeno quimérico más básico generalmente se forma mediante la fusión del dominio de unión al antígeno tumoral extracelular y la cadena CD3-ζ intracelular. El primero puede ayudar a que las células T se dirijan a los tumores y el segundo puede proporcionar señales de iniciación inmunológica.
Entonces hay dos formas de mejorar la función de CAR-T. Uno es aumentar el área de reconocimiento de antígenos extracelulares para mejorar la capacidad de cazar tumores; el otro es mejorar las señales internas para mantener el crecimiento y el metabolismo de las células T. Deja que exista en el cuerpo por más tiempo.
El primero es más fácil de entender, porque generalmente hay una variedad de antígenos en la superficie de las células tumorales, y las células CAR-T generalmente pueden reconocer algunos de estos antígenos después de la modificación para atacar el objetivo. Solo necesitamos agregar objetivos externos que ataquen diferentes antígenos al mismo tiempo para mejorar la capacidad anticancerígena de CAR-T. Este es también el concepto CAR-T de doble focalización que ha surgido recientemente.
En comparación con las células CAR-T que reconocen solo un antígeno, estas células T de doble objetivo pueden rastrear el paradero de las células cancerosas de manera más eficiente y evitar que eviten el sistema inmunológico.
Para la modificación interna, en las últimas generaciones de iteraciones de actualización de la tecnología CAR, los receptores de antígenos quiméricos básicamente han agregado algunas moléculas coestimuladoras, incluidas CD28 y 4-1BB, etc., las moléculas coestimuladoras pueden mantener y mejorar la función CAR-T y la capacidad de proliferación.
Sin embargo, estudios anteriores que utilizaron una sola molécula coestimuladora en receptores quiméricos de doble diana han encontrado que esto no puede controlar el crecimiento tumoral durante mucho tiempo, ni puede resolver el problema de los tumores sólidos. Por lo tanto, el equipo de investigación de la Universidad de Carolina del Norte decidió introducir las señales de dos moléculas coestimuladoras al mismo tiempo y llevarlas a diferentes receptores de doble objetivo para promover aún más la capacidad de las células CAR-T.
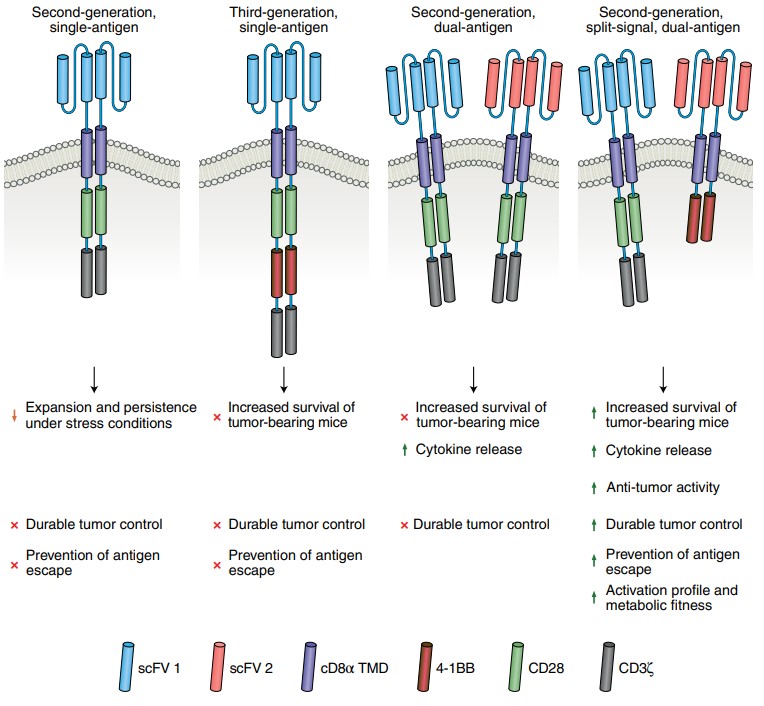
El estudio utilizó el neuroblastoma como objetivo de prueba, y las células CAR-T también llevan las regiones de unión a la diana de los antígenos tumorales GD2 y B7-H3, y los dos receptores quiméricos llevan cada uno una molécula coestimuladora CD28 o 4-1BB. Este CAR-T de doble señal y doble objetivo puede destruir completamente las células in vitro después de ser cocultivado con neuroblastoma.
En el experimento con ratones, los investigadores introdujeron células de neuroblastoma en los ratones, y los ratones que usaban un solo antígeno diana sufrirían la reaparición del tumor poco después. Sin embargo, las generaciones anteriores de métodos CAR-T no pueden prevenir el proceso de recurrencia del tumor. Solo las células CAR-T de doble señal y doble objetivo pueden lograr este objetivo y controlar el crecimiento tumoral.
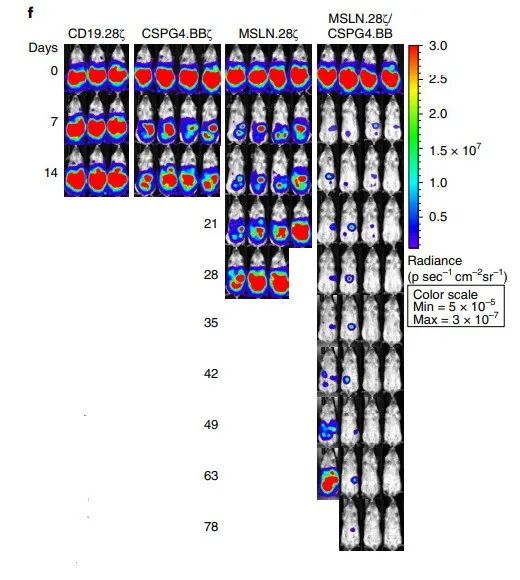
Y los ratones que reciben la nueva terapia aún pueden lograr el efecto de control del tumor incluso si se someten al proceso de reestimulación del tumor. Los resultados de la prueba muestran que después de 2 y 4 semanas de tratamiento, todavía se pueden detectar altos niveles de células CAR-T de doble señal y doble objetivo en los ratones. Esto significa que estas células pueden durar para siempre en el cuerpo.
De los resultados de la prueba, esta ventaja puede provenir de la ayuda mutua de las dos señales en la celda. Por ejemplo, el receptor quimérico de CD28 y 4-1BB puede mejorar el efecto de señal de CD3-ζ y potenciar el metabolismo y la proliferación de las células T.
En general, el estudio proporciona una nueva idea del uso de CAR-T para resolver tumores sólidos. Sin embargo, las moléculas coestimuladoras específicas que se utilizarán deben determinarse de acuerdo con diferentes entornos tumorales.